高等真菌由于特殊的生长方式和在生态环境中的重要作用,能够产生结构新颖多样并且具有良好生物活性的化合物,这些天然产物为药物和生物农药的开发提供了先导资源,例如杀菌剂strobilurins (嗜球果伞素)、抗生素pleuromutilins (截短侧耳素)、抗肿瘤的illudins (隐杯伞素)、抑制线虫的omphalotins等。随着基因组测序和生物信息技术的发展,天然产物生物合成研究取得了突破性的进展。但由于受遗传背景复杂、遗传操作困难等因素的制约,高等真菌天然产物的生物合成研究一直落后于细菌及低等真菌(Front. Microbiol. 2015, 6, 127.)。
中国科学院昆明植物研究所植物化学与西部植物资源持续利用国家重点实验室曾英研究组近年来同刘吉开研究组合作,致力于高等真菌次生代谢与天然产物的生物合成研究。前期揭示了新颖的胰脂肪酶抑制剂韧革菌素Vibralactone在褐盖韧革菌 (Boreostereum vibrans) 中的生成途径,证明韧革菌素罕见的4/5融合双环内酯骨架既不是聚酮也不是倍半萜来源,而是由莽草酸途径的芳环衍生而来(德国应用化学Angewandte Chemie International Edition 2013, 52: 2298–2302)。韧革菌素奇妙的生物合成途径,充分显示了高等真菌非凡的创造力。
最近,博士生杨彦龙等研究人员综合运用有机化学以及生化与分子生物学技术,通过前体指导的生物合成,进一步研究了褐盖韧革菌中结构多样的混源萜类化合物的生物合成机制(图1)。首次在基因与酶学水平上确定了参与其中氧化脱羧关键反应的单氧化酶VibMO1(图2),从而证实了长久以来的推测:异戊烯基取代的对苯二酚类化合物(有时也称之为混源萜meroterpenoids)很可能来源于异戊烯基取代的对羟基苯甲酸的氧化脱羧。单氧化酶VibMO1的发现,还为真核生物辅酶Q形成过程中催化类似反应的酶基因鉴定提供了重要线索。同时,该研究还证明了由异戊烯基对羟基苯甲醇通过发散生物合成途径(a divergent pathway)形成韧革菌素类混源萜(图3),其中3-取代的γ丁内酯类化合物Vibralactone G (8)新颖的生物合成途径,还是首次在天然产物化学中报道。研究结果加深了对次生代谢产物结构多样性产生机制的认识,为天然产物的生物合成研究开辟了新的视野。此外,硕士生周慧等研究人员还从褐盖韧革菌克隆鉴定了能够催化FPP形成以δ-cadinol为主产物的倍半萜合酶BvCS(图4),该酶很有可能参与褐盖韧革菌倍半萜Boreovibrins的生物合成。
以上研究成果分别以“A Monooxygenase from Boreostereum vibrans Catalyzes Oxidative Decarboxylation in a Divergent Vibralactone Biosynthesis Pathway” 和 “Identification and Characterization of a δ-Cadinol Synthase Potentially Involved in the Formation of Boreovibrins in Boreostereum vibrans of Basidiomycota”为题发表在化学类顶尖期刊Angewandte Chemie International Edition (《德国应用化学》 2016, 55: 5463–5466;http://onlinelibrary.wiley.com/doi/10.1002/anie.201510928/full ),及Natural Products and Bioprospecting (2016, http://link.springer.com/article/10.1007/s13659-016-0096-4)。特别感谢本所分析测试中心杨静博士通过计算化学确定化合物11a的绝对构型。
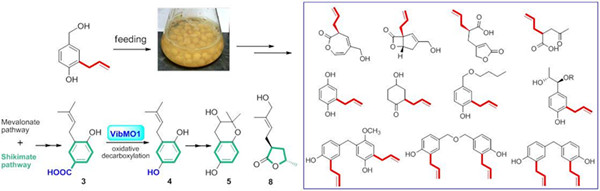
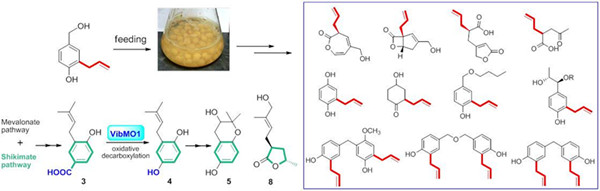
图1. 褐盖韧革菌的次生代谢与发散生物合成途径(Divergent Biosynthesis Pathway)


图2. A) 褐盖韧革菌单氧化酶VibMO1的鉴定;B) VibMO1同源酶及其关联的真菌天然产物
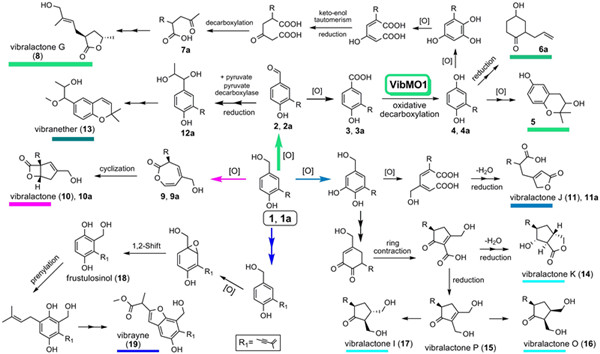

图3. 通过发散生物合成途径从异戊烯基对羟基苯甲醇形成韧革菌素类混源萜 (R=allyl for analogues with compound designations containing a; R=prenyl for natural products)
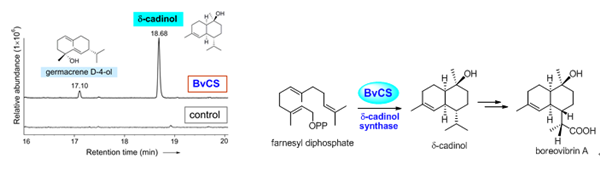
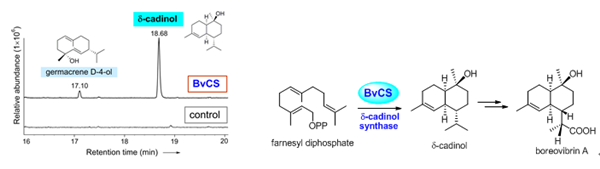
图4. 褐盖韧革菌倍半萜合酶BvCS催化FPP形成主产物δ-cadinol